Tabla de contenido para este artículo:
1. Desarrollo de aminoácidos
2. Propiedades estructurales
3. Composición química
4. clasificación
5. Síntesis
6. Propiedades fisicoquímicas
7. Toxicidad
8. Actividad antimicrobiana
9. Propiedades reológicas
10. Aplicaciones en la industria cosmética
11. Aplicaciones en cosméticos cotidianos
Tensioactivos de aminoácidos (AAS)son una clase de tensioactivos formados mediante la combinación de grupos hidrofóbicos con uno o más aminoácidos. En este caso, los aminoácidos pueden ser sintéticos o derivados de hidrolizados de proteínas o fuentes renovables similares. Este documento cubre los detalles de la mayoría de las rutas sintéticas disponibles para AAS y el efecto de diferentes rutas en las propiedades fisicoquímicas de los productos finales, incluida la solubilidad, la estabilidad de dispersión, la toxicidad y la biodegradabilidad. Como clase de tensioactivos para aumentar la demanda, la versatilidad de AAS debido a su estructura variable ofrece una gran cantidad de oportunidades comerciales.
Dado que los tensioactivos se usan ampliamente en detergentes, emulsionantes, inhibidores de la corrosión, recuperación del aceite terciario y productos farmacéuticos, los investigadores nunca han dejado de prestar atención a los tensioactivos.
Los tensioactivos son los productos químicos más representativos que se consumen en grandes cantidades a diario en todo el mundo y han tenido un impacto negativo en el entorno acuático.Los estudios han demostrado que el uso generalizado de los tensioactivos tradicionales puede tener un impacto negativo en el medio ambiente.
Hoy, la no toxicidad, la biodegradabilidad y la biocompatibilidad son casi tan importantes para los consumidores como la utilidad y el rendimiento de los tensioactivos.
Los biosurfactantes son tensioactivos sostenibles respetuosos con el medio ambiente que se sintetizan naturalmente por microorganismos como bacterias, hongos y levadura, o se secretan extracelularmente.Por lo tanto, los biosurfactantes también se pueden preparar mediante diseño molecular para imitar estructuras anfifílicas naturales, como fosfolípidos, glucósidos de alquilo y aminoácidos acilo.
Tensioactivos de aminoácidos (AAS)son uno de los tensioactivos típicos, generalmente producidos a partir de materias primas derivadas de animales o agrícolas. En las últimas dos décadas, AAS ha atraído un gran interés de los científicos como tensioactivos novedosos, no solo porque pueden sintetizarse de los recursos renovables, sino también porque los AA son fácilmente degradables y tienen subproductos inofensivos, haciéndolos más seguros para el medio ambiente.
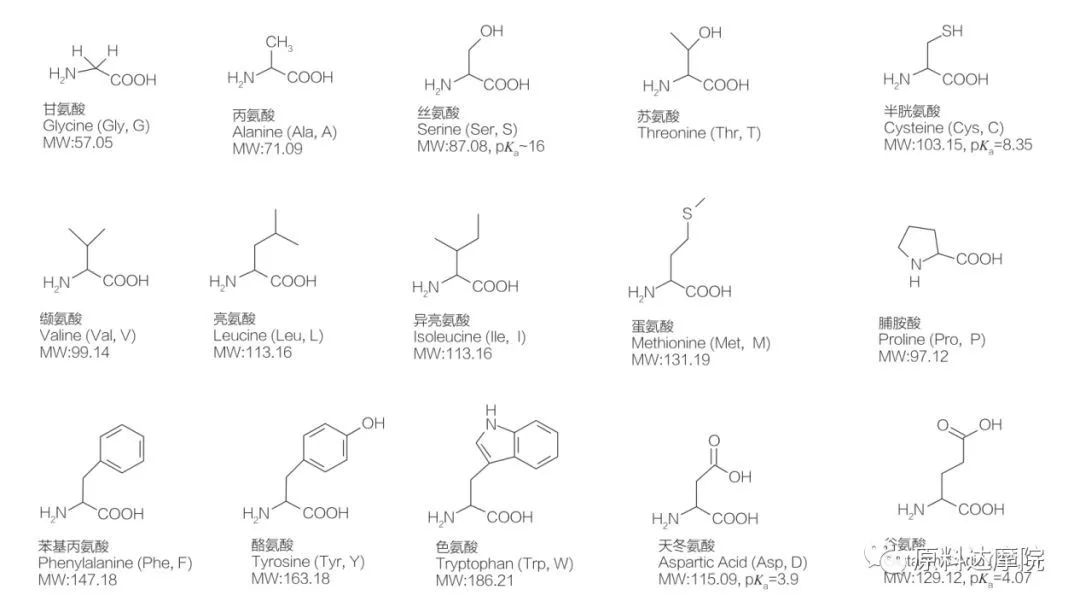
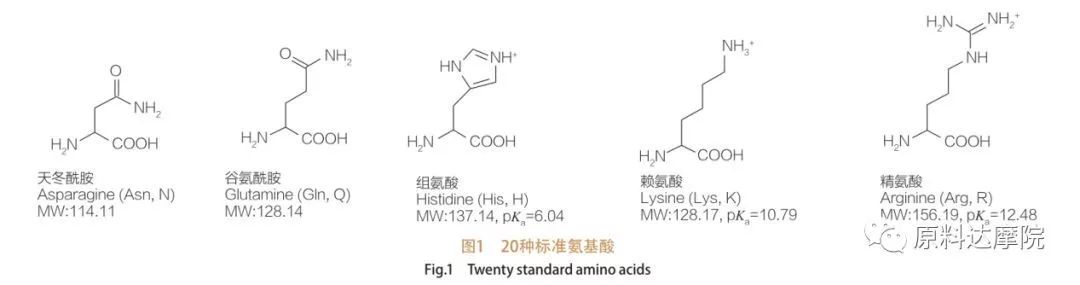
AAS se puede definir como una clase de tensioactivos que consisten en aminoácidos que contienen grupos de aminoácidos (HO 2 C-CHR-NH 2) o residuos de aminoácidos (HO 2 C-CHR-NH-). Las 2 regiones funcionales de aminoácidos permiten la derivación de una amplia variedad de tensioactivos. Se sabe que un total de 20 aminoácidos proteinogénicos estándar existen en la naturaleza y son responsables de todas las reacciones fisiológicas en el crecimiento y las actividades de la vida. Se diferencian entre sí solo según el residuo R (Figura 1, PK A es el logaritmo negativo de la constante de disociación ácida de la solución). Algunos no son polares e hidrofóbicos, otros son polares e hidrófilos, otros son básicos y otros son ácidos.
Debido a que los aminoácidos son compuestos renovables, los tensioactivos sintetizados a partir de aminoácidos también tienen un alto potencial para volverse sostenibles y respetuosos con el medio ambiente. La estructura simple y natural, la baja toxicidad y la biodegradabilidad rápida a menudo los hacen superiores a los tensioactivos convencionales. Utilizando materias primas renovables (por ejemplo, aminoácidos y aceites vegetales), AAS puede ser producido por diferentes rutas biotecnológicas y rutas químicas.
A principios del siglo XX, se descubrió que los aminoácidos se usaron primero como sustratos para la síntesis de tensioactivos.Los AA se usaron principalmente como conservantes en formulaciones farmacéuticas y cosméticas.Además, se descubrió que los AA eran biológicamente activos contra una variedad de bacterias, tumores y virus que causan enfermedades. En 1988, la disponibilidad de AAS de bajo costo generó interés de investigación en la actividad superficial. Hoy, con el desarrollo de la biotecnología, algunos aminoácidos también pueden sintetizarse comercialmente a gran escala por levadura, lo que demuestra indirectamente que la producción de AAS es más ecológica.
01 Desarrollo de aminoácidos
Ya a principios del siglo XIX, cuando se descubrieron los aminoácidos naturales por primera vez, se predijo que sus estructuras eran extremadamente valiosas, utilizables como materias primas para la preparación de anfifílicos. Bondi informó el primer estudio sobre la síntesis de AAS en 1909.
En ese estudio, la N-acilglicina y la N-acilalanina se introdujeron como grupos hidrofílicos para tensioactivos. El trabajo posterior implicó la síntesis de lipoaminoácidos (AAS) usando glicina y alanina, y Hentrich et al. publicó una serie de hallazgos,incluyendo la primera aplicación de patente, sobre el uso de sales de acil sarcosinato y acilo aspartato como tensioactivos en productos de limpieza doméstica (por ejemplo, champús, detergentes y pastas de dientes).Posteriormente, muchos investigadores investigaron la síntesis y las propiedades fisicoquímicas de los aminoácidos de acilo. Hasta la fecha, se ha publicado un gran cuerpo de literatura sobre la síntesis, propiedades, aplicaciones industriales y biodegradabilidad de AAS.
02 Propiedades estructurales
Las cadenas de ácidos grasos hidrofóbicos no polares de AAS pueden variar en estructura, longitud de la cadena y número.La diversidad estructural y la alta actividad superficial de AAS explican su amplia diversidad compositiva y sus propiedades fisicoquímicas y biológicas. Los grupos de cabeza de AAS están compuestos de aminoácidos o péptidos. Las diferencias en los grupos de cabeza determinan la adsorción, la agregación y la actividad biológica de estos tensioactivos. Los grupos funcionales en el grupo principal determinan el tipo de AAS, incluidos los catiónicos, aniónicos, no iónicos y anfotéricos. La combinación de aminoácidos hidrofílicos y porciones hidrofóbicas de cadena larga forman una estructura anfifílica que hace que la molécula sea altamente activa en la superficie. Además, la presencia de átomos de carbono asimétricos en la molécula ayuda a formar moléculas quirales.
03 composición química
Todos los péptidos y polipéptidos son los productos de polimerización de estos casi 20 α-amino α-aminoácidos α. Todos los 20 α-aminoácidos contienen un grupo funcional de ácido carboxílico (-COOH) y un grupo funcional amino (-nh 2), ambos unidos al mismo átomo de carbono α-carbono tetraédrico. Los aminoácidos difieren entre sí por los diferentes grupos R unidos al α-carbono (a excepción de la licina, donde el grupo R es hidrógeno). Los grupos R pueden diferir en estructura, tamaño y carga (acidez, alcalinidad). Estas diferencias también determinan la solubilidad de los aminoácidos en el agua.
Los aminoácidos son quirales (a excepción de la glicina) y son ópticamente activos por naturaleza porque tienen cuatro sustituyentes diferentes vinculados al carbono alfa. Los aminoácidos tienen dos conformaciones posibles; Son imágenes de espejo no superpuestas entre sí, a pesar del hecho de que el número de L-Stereoisómeros es significativamente mayor. El grupo R presente en algunos aminoácidos (fenilalanina, tirosina y triptófano) es arilo, lo que conduce a una absorción UV máxima a 280 nm. El α-COOH ácido y el α-NH 2 básico en los aminoácidos son capaces de ionización, y ambos estereoisómeros, que sean, construyen el equilibrio de ionización que se muestra a continuación.
R-COOH ↔R-COO-+ H+
R-NH3+↔r-nh2+ H+
Como se muestra en el equilibrio de ionización anterior, los aminoácidos contienen al menos dos grupos débilmente ácidos; Sin embargo, el grupo carboxilo es mucho más ácido en comparación con el grupo amino protonado. PH 7.4, el grupo carboxilo se desprotona mientras el grupo amino se protona. Los aminoácidos con grupos R no ionizables son eléctricamente neutrales a este pH y forman zwitterion.
04 Clasificación
AAS se puede clasificar de acuerdo con cuatro criterios, que se describen a continuación a su vez.
4.1 Según el origen
| Según el origen, AAS se puede dividir en 2 categorías de la siguiente manera. ① Categoría natural Algunos compuestos naturales que contienen aminoácidos también tienen la capacidad de reducir la tensión superficial/interfacial, y otros incluso exceden la eficacia de los glucolípidos. Estos AA también se conocen como lipopéptidos. Los lipopéptidos son compuestos de bajo peso molecular, generalmente producidos por especies de Bacillus.
Tales AA se dividen aún más en 3 subclases:tensioactina, iturina y fengicina.
|
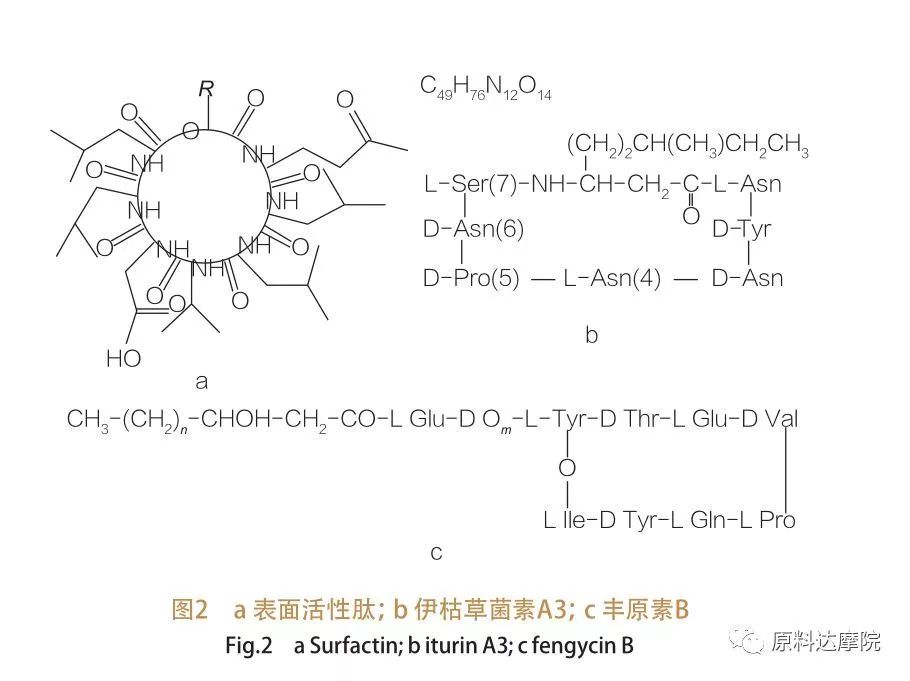
| La familia de péptidos activos de superficie abarca las variantes de heptapéptidos de una variedad de sustancias,Como se muestra en la Figura 2A, en la que una cadena de ácido graso β-hidroxi insaturado C12-C16 está vinculada al péptido. El péptido de superficie activo es una lactona macrocíclica en la que el anillo está cerrado por catálisis entre el extremo C del ácido graso β-hidroxi y el péptido. En la subclase de la iturina, hay seis variantes principales, a saber, iturina A y C, micosubtilina y bacilomicina D, F y L.En todos los casos, los heptapéptidos están vinculados a las cadenas C14-C17 de ácidos grasos β-amino (las cadenas pueden ser diversas). En el caso de las ekurimicinas, el grupo amino en la posición β puede formar un enlace de amida con el terminal C, formando así una estructura de lactama macrocíclico.
La fengicina subclase contiene fengicina A y B, que también se llama plipastatina cuando Tyr9 está configado.El decapéptido está relacionado con una cadena de ácidos grasos β -hidroxi saturados o insaturados C14 -C18. Estructuralmente, la plipastatina también es una lactona macrocíclica, que contiene una cadena lateral de Tyr en la posición 3 de la secuencia de péptidos y forman un enlace éster con el residuo C-terminal, formando así una estructura de anillo interno (como es el caso de muchos lipopéptidos de Pseudomonas).
② Categoría sintética AAS también se puede sintetizar utilizando cualquiera de los aminoácidos ácidos, básicos y neutros. Los aminoácidos comunes utilizados para la síntesis de AAS son ácido glutámico, serina, prolina, ácido aspártico, glicina, arginina, alanina, leucina e hidrolizados de proteínas. Esta subclase de tensioactivos puede prepararse mediante métodos químicos, enzimáticos y quimioenzimáticos; Sin embargo, para la producción de AAS, la síntesis química es más factible económicamente. Los ejemplos comunes incluyen ácido N-lauroil-L-glutámico y ácido N-palmitoil-L-glutámico.
|
4.2 Basado en sustituyentes de cadena alifática
Según los sustituyentes de la cadena alifática, los tensioactivos a base de aminoácidos se pueden dividir en 2 tipos.
Según la posición del sustituyente
| ①N-sustituido AAS En los compuestos N-sustituidos, un grupo amino se reemplaza por un grupo lipofílico o un grupo carboxilo, lo que resulta en una pérdida de basicidad. El ejemplo más simple de los AA de N-sustituido son los aminoácidos N-acil, que son esencialmente tensioactivos aniónicos. Los AA de N-sustituido tienen un enlace de amida unido entre las porciones hidrofóbicas e hidrofílicas. El enlace de amida tiene la capacidad de formar un enlace de hidrógeno, que facilita la degradación de este tensioactivo en un entorno ácido, lo que lo hace biodegradable.
②c-sustituido AAS En los compuestos sustituidos en C, la sustitución ocurre en el grupo carboxilo (a través de un enlace amida o éster). Los compuestos típicos de C-sustituidos (por ejemplo, ésteres o amidas) son esencialmente tensioactivos catiónicos.
③N y C-sustituido AAS En este tipo de tensioactivo, los grupos amino y carboxilo son la parte hidrofílica. Este tipo es esencialmente un tensioactivo anfotérico. |
4.3 Según el número de colas hidrofóbicas
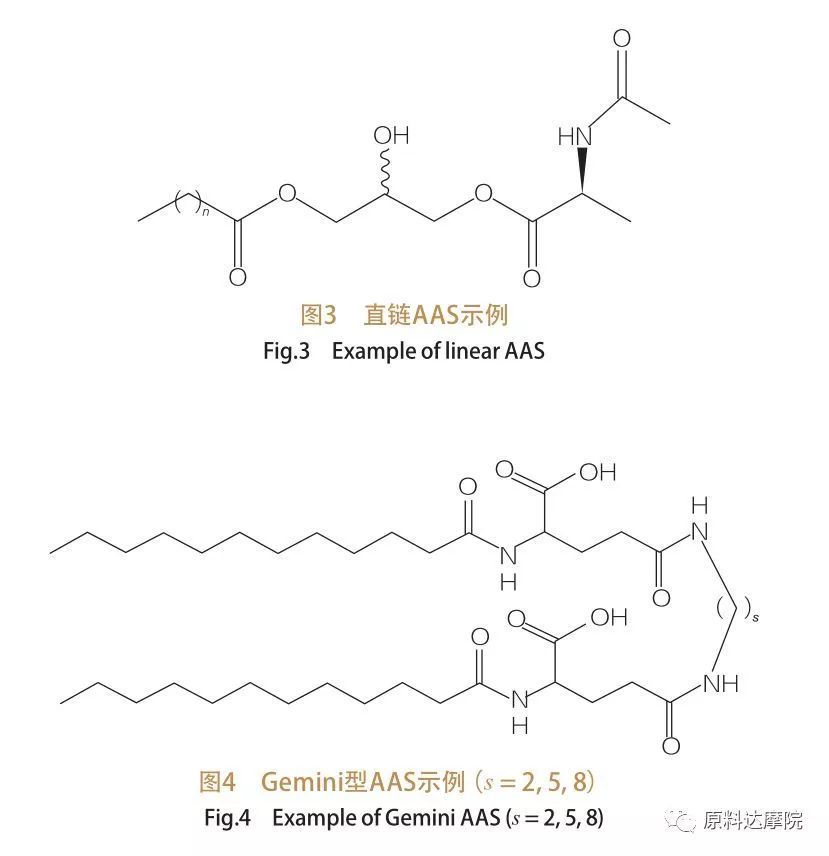
Según el número de grupos de cabeza y las colas hidrofóbicas, AAS se puede dividir en cuatro grupos. AAS de cadena recta, Géminis (dímero) Tipo AAS, Glicerolipid Tipo AAS y Bicifalic Amphifilic (Bola) tipo AAS. Los tensioactivos de cadena recta son tensioactivos que consisten en aminoácidos con solo una cola hidrofóbica (Figura 3). Géminis tipo AAS tiene dos grupos de cabeza polar de aminoácidos y dos colas hidrófobas por molécula (Figura 4). En este tipo de estructura, los dos AA de cadena recta están unidos por un espaciador y, por lo tanto, también se llaman dímeros. En el tipo AAS de glicerolípidos, por otro lado, las dos colas hidrofóbicas están unidas al mismo grupo de cabeza de aminoácidos. Estos tensioactivos pueden considerarse como análogos de monoglicéridos, diglicéridos y fosfolípidos, mientras que en AAS de tipo bola, dos grupos de cabeza de aminoácidos están unidos por una cola hidrofóbica.
4.4 Según el tipo de grupo principal
① AAS CCATIONIC
El grupo principal de este tipo de tensioactivo tiene una carga positiva. La AAS catiónica más temprana es el etil cocoil arginato, que es un carboxilato de pirrolidona. Las propiedades únicas y diversas de este tensioactivo lo hacen útil en desinfectantes, agentes antimicrobianos, agentes antiestáticos, acondicionadores del cabello, así como ser suave con los ojos y la piel y fácilmente biodegradables. Singare y Mhatre sintetizaron AA catiónicos basados en arginina y evaluaron sus propiedades fisicoquímicas. En este estudio, reclamaron altos rendimientos de los productos obtenidos utilizando condiciones de reacción de Schotten-Baumann. Con el aumento de la longitud de la cadena alquilo y la hidrofobicidad, se encontró que la actividad superficial del tensioactivo aumenta y la concentración crítica de micelas (CMC) disminuirá. Otro es la proteína acil cuaternaria, que se usa comúnmente como acondicionador en productos para el cuidado del cabello.
②Asiónico AAS
En los tensioactivos aniónicos, el grupo de cabeza polar del surfactante tiene una carga negativa. La sarcosina (CH 3 -NH -CH 2 -COOH, N -metilglicina), un aminoácido que se encuentra comúnmente en los erizos de mar y las estrellas de mar, está químicamente relacionado con la glicina (NH 2 -Ch 2 -CoOH,), un aminoácido básico que se encuentra en las células de mamíferos. -Cooh,) está químicamente relacionado con la glicina, que es un aminoácido básico que se encuentra en las células de mamíferos. El ácido láurico, el ácido tetradecanoico, el ácido oleico y sus haluros y ésteres se usan comúnmente para sintetizar tensioactivos de sarcosinato. Los sarcosinatos son inherentemente suaves y, por lo tanto, se usan comúnmente en enjuagues bucales, champús, espumas de afeitar, protectores solares, limpiadores de la piel y otros productos cosméticos.
Otros AA aniónicos disponibles comercialmente incluyen Amisoft CS-22 y AmilitegCK-12, que son nombres comerciales para el n-cococil-l-glutamato de sodio y el glicinato N-cocoil de potasio, respectivamente. La amilita se usa comúnmente como agente espumante, detergente, solubilizante, emulsionante y dispersante, y tiene muchas aplicaciones en cosméticos, como champús, jabones de baño, lavados corporales, pastas de dientes, limpiadores faciales, jabones de limpieza, limpiadores de lentes y surfactantes domésticos. Amisoft se usa como un limpiador suave para la piel y el cabello, principalmente en limpiadores faciales y corporales, bloquea detergentes sintéticos, productos para el cuidado del cuerpo, champús y otros productos para el cuidado de la piel.
③zwitteriónico o anfotérico AAS
Los tensioactivos anfotéricos contienen sitios ácidos y básicos y, por lo tanto, pueden cambiar su carga cambiando el valor de pH. En medios alcalinos se comportan como tensioactivos aniónicos, mientras que en entornos ácidos se comportan como tensioactivos catiónicos y en medios neutros como tensioactivos anfotéricos. Lauril lisina (LL) y el alcoxi (2-hidroxipropil) arginina son los únicos tensioactivos anfotéricos conocidos basados en aminoácidos. LL es un producto de condensación de lisina y ácido lauric. Debido a su estructura anfotérica, LL es insoluble en casi todos los tipos de solventes, excepto para solventes muy alcalinos o ácidos. Como polvo orgánico, LL tiene una excelente adhesión a las superficies hidrofílicas y un bajo coeficiente de fricción, dando a este tensioactivo una excelente capacidad de lubricante. LL se usa ampliamente en cremas para la piel y acondicionadores para el cabello, y también se usa como lubricante.
④AsNoniónico AAS
Los tensioactivos no iónicos se caracterizan por grupos de cabeza polar sin cargos formales. Al-Sabagh et al. de α-aminoácidos solubles en aceite. En este proceso, la L-fenilalanina (LEP) y la L-leucina se esterificaron primero con hexadecanol, seguido de una amabilidad con ácido palmítico para dar dos amidas y dos ésteres de α-aminoácidos. Los amidos y los ésteres se sometieron a reacciones de condensación con óxido de etileno para preparar tres derivados de fenilalanina con diferentes números de unidades de polioxietileno (40, 60 y 100). Se descubrió que estos AA no iónicos tienen una buena detergencia y propiedades de espuma.
05 Síntesis
5.1 Ruta sintética básica
En AAS, los grupos hidrofóbicos se pueden unir a sitios de amina o ácido carboxílico, o a través de las cadenas laterales de aminoácidos. Según esto, hay cuatro rutas sintéticas básicas disponibles, como se muestra en la Figura 5.
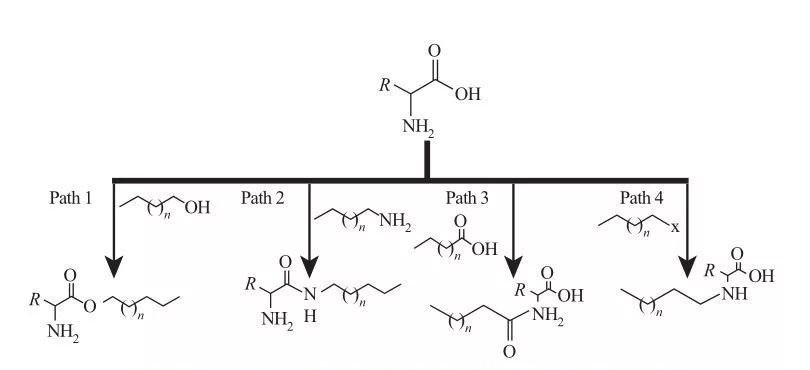
Fig.5 Caminos de síntesis fundamentales de tensioactivos a base de aminoácidos
| Camino 1. Las aminas de éster anfifílico se producen mediante reacciones de esterificación, en cuyo caso la síntesis de tensioactivo generalmente se logra mediante reflujo de alcoholes grasos y aminoácidos en presencia de un agente deshidratante y un catalizador ácido. En algunas reacciones, el ácido sulfúrico actúa como un catalizador y un agente deshidratante.
Camino 2. Los aminoácidos activados reaccionan con las alquilaminas para formar enlaces de amida, lo que resulta en la síntesis de amidoaminas anfifílicas.
Camino 3. Los amido ácidos se sintetizan reaccionando los grupos amina de aminoácidos con amido ácidos.
Camino 4. Los aminoácidos alquilo de cadena larga se sintetizaron mediante la reacción de grupos de amina con haloalcanos. |
5.2 Avances en síntesis y producción
5.2.1 Síntesis de tensioactivos de aminoácidos/péptidos de cadena única
Los aminoácidos o péptidos de N-acil o o-acil se pueden sintetizar mediante acilación catalizada por enzimas de grupos amina o hidroxilo con ácidos grasos. El primer informe sobre la síntesis catalizada por lipasa sin solventes de amida amida o derivados de éster metílico utilizaron la antártica Candida, con rendimientos que varían de 25% a 90% dependiendo del aminoácido objetivo. La metil etil cetona también se ha utilizado como solvente en algunas reacciones. Vonderhagen et al. También describió las reacciones de N-Ayedleation catalizadas por la lipasa y la proteasa de los aminoácidos, los hidrolizados de proteínas y/o sus derivados utilizando una mezcla de agua y solventes orgánicos (p. Ej., Dimetilformamida/agua) y metil ketona.
En los primeros días, el principal problema con la síntesis catalizada por enzimas de AAS fueron los bajos rendimientos. Según Valivety et al. El rendimiento de los derivados de aminoácidos N-tetradecanoil fue de solo 2% -10% incluso después de usar diferentes lipasas e incubar a 70 ° C durante muchos días. Montet et al. También encontró problemas con respecto al bajo rendimiento de aminoácidos en la síntesis de N-acil lisina utilizando ácidos grasos y aceites vegetales. Según ellos, el rendimiento máximo del producto fue del 19% en condiciones sin solventes y utilizando solventes orgánicos. El mismo problema fue encontrado por Valivety et al. En la síntesis de derivados de éster metílico N-CBZ-L-lisina o N-CBZ-lisina.
En este estudio, afirmaron que el rendimiento de 3-O-tetradecanoil-L-serina fue del 80% cuando se usa serina protegida con N como sustrato y novozima 435 como catalizador en un entorno sin solventes fundidos. Nagao y Kito estudiaron la aclación de L-serina, L-homoserina, L-treonina y L-tirosina (let) Al usar la lipasa de los resultados de la reacción (Lipasa se obtuvo por Candida cylindracea y Rhizopus delemar en el medio acuoso) e informaron que los cilindros de acilación de L-homoserinos y L-Homosings y L-Sserine fueron algunos que se aleman. Acilación de L-treonina y se produjo.
Muchos investigadores han apoyado el uso de sustratos económicos y fácilmente disponibles para la síntesis de AAS rentables. Soo et al. afirmó que la preparación de tensioactivos a base de aceite de palma funciona mejor con lipoenzima inmovilizada. Señalaron que el rendimiento de los productos sería mejor a pesar de la reacción que lleva mucho tiempo (6 días). Gerova et al. investigó la síntesis y la actividad superficial de N-palmitoil AAS quiral basado en metionina, prolina, leucina, treonina, fenilalanina y fenilglicina en una mezcla cíclica/racémica. Pang y Chu describieron la síntesis de monómeros a base de aminoácidos y monómeros basados en ácido dicarboxílico en solución, se sintetizaron una serie de ésteres de poliamida basados en aminoácidos funcionales y biodegradables por reacciones de co-condensación en solución.
Cantaeuzene y Guerreiro informaron la esterificación de los grupos de ácido carboxílico de BOC-ALA-OH y BOC-ASP-OH con alcoholes y diolos alifáticos de cadena larga, con diclorometano como solvente y agarosa 4B (Sepharosa 4B) como catalizador. En este estudio, la reacción de BOC-ALA-OH con alcoholes grasos de hasta 16 carbonos dio buenos rendimientos (51%), mientras que para BOC-ASP-OH 6 y 12 carbonos fueron mejores, con un rendimiento correspondiente del 63% [64]. 99.9%) en rendimientos que van del 58%al 76%, que se sintetizaron mediante la formación de enlaces de amida con varias alquilaminas de cadena larga o enlaces de éster con alcoholes grasos por CBZ-Arg-OMO, donde la papaína actuó como un catalizador.
5.2.2 Síntesis de tensioactivos de aminoácidos/péptidos a base de Géminis
Los tensioactivos de Géminis basados en aminoácidos consisten en dos moléculas AAS de cadena recta unidas entre sí por un grupo espaciador. Hay 2 posibles esquemas para la síntesis quimioenzimática de tensioactivos a base de aminoácidos de tipo Gemini (Figuras 6 y 7). En la Figura 6, se reaccionan 2 derivados de aminoácidos con el compuesto como grupo espaciador y luego se introducen 2 grupos hidrofóbicos. En la Figura 7, las 2 estructuras de cadena recta están directamente unidas por un grupo espaciador bifuncional.
El desarrollo más temprano de la síntesis catalizada por enzimas de los lipoaminoácidos de Géminis fue pionero por Valivety et al. Yoshimura et al. investigó la síntesis, adsorción y agregación de un tensioactivo Géminis basado en aminoácidos basado en cistina y bromuro de N-alquilo. Los tensioactivos sintetizados se compararon con los tensioactivos monoméricos correspondientes. Faustino et al. describió la síntesis de AA monoméricos aniónicos basados en urea basada en L-cystine, d-cystine, dl-cistine, l-cisteína, L-metionina y L-sulfoalanina y sus pares de gemini por medio de conductividad, tensión de la superficie de equilibrio y la caracterización de fluorescencia en estados en estado de ellos. Se demostró que el valor CMC de Géminis era más bajo comparando Monómero y Géminis.
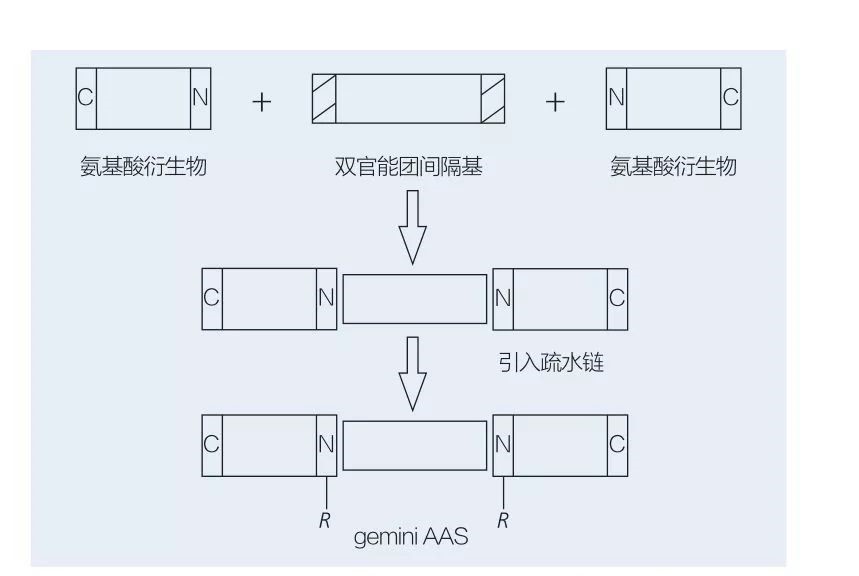
Fig.6 Síntesis de Géminis AAS usando derivados y espaciadores AA, seguido de inserción del grupo hidrófobo
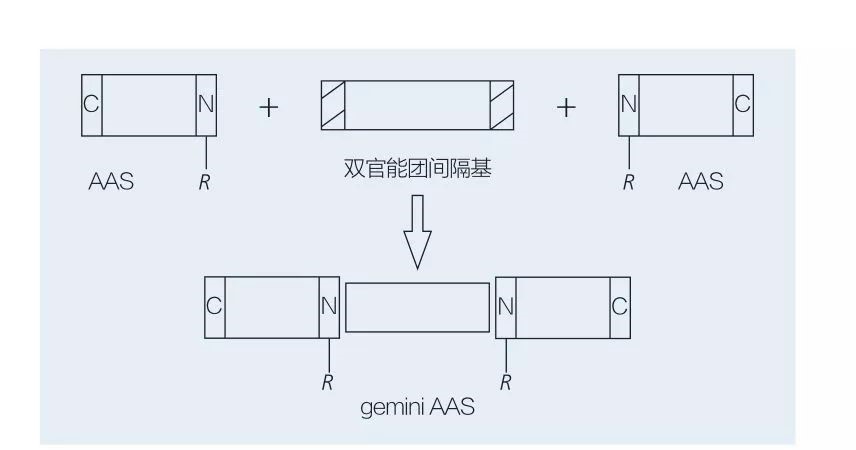
Fig.7 Síntesis de Géminis Aass usando espaciador bifuncional y AAS
5.2.3 Síntesis de tensioactivos de aminoácidos/péptidos glicerolípidos
Los tensioactivos de aminoácidos/péptidos glicerolípidos son una nueva clase de aminoácidos lipídicos que son análogos estructurales de los ésteres mono- (o di) de glicerol y los fosfolípidos, debido a su estructura de una o dos cadenas de grasas con un aminoácido unido a la fapa del glicerol por un vínculo de éster. La síntesis de estos tensioactivos comienza con la preparación de ésteres de glicerol de aminoácidos a temperaturas elevadas y en presencia de un catalizador ácido (por ejemplo, BF 3). La síntesis catalizada por enzimas (usando hidrolasas, proteasas y lipasas como catalizadores) también es una buena opción (Figura 8).
Se ha informado la síntesis catalizada por enzimas de conjugados de glicéridos de arginina dilatilados que usan papaína. La síntesis de conjugados éster de diacilglicerol a partir de acetilarginina y la evaluación de sus propiedades fisicoquímicas también se ha informado.
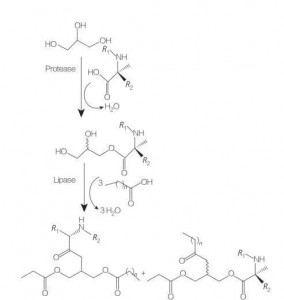
Fig.8 Síntesis de conjugados de aminoácidos mono y diacilglicerol
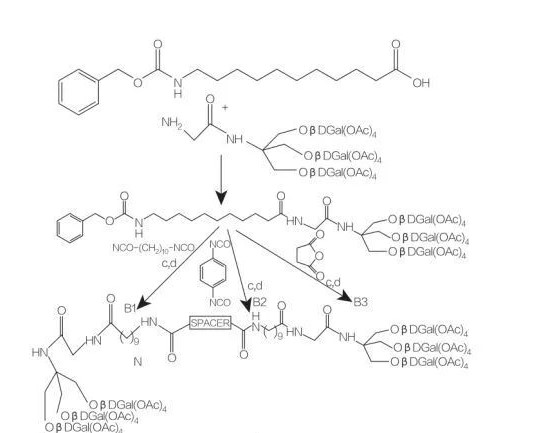
espaciador: NH- (CH2)10-Nh: compuestob1
espaciador: NH-C6H4-Nh: compuestob2
espaciador: CH2-Ch2: compuestob3
Fig.
5.2.4 Síntesis de tensioactivos de aminoácidos/péptidos a base de bola
Los anfifiles de tipo bola a base de aminoácidos contienen 2 aminoácidos que están vinculados a la misma cadena hidrófoba. Franceschi et al. describió la síntesis de anfifiles de tipo bola con 2 aminoácidos (D- o L-alanina o L-histidina) y 1 cadena alquilo de diferentes longitudes e investigó su actividad superficial. Discuten la síntesis y la agregación de nuevos anfifílicos de tipo bola con una fracción de aminoácidos (usando un β-aminoácido poco común o un alcohol) y un grupo espaciador C12 -C20. Los β-aminoácidos poco comunes utilizados pueden ser un aminoácido de azúcar, un aminoácido derivado de azidotimina (AZT), un aminoácido norbornene y un alcohol amino derivado de AZT (Figura 9). La síntesis de los anfifiles simétricos de tipo bola derivados de Tris (hidroximetil) aminometano (Tris) (Figura 9).
06 Propiedades fisicoquímicas
Es bien sabido que los tensioactivos a base de aminoácidos (AA) son de naturaleza diversa y versátil y tienen una buena aplicabilidad en muchas aplicaciones, como una buena solubilización, buenas propiedades de emulsificación, alta eficiencia, alto rendimiento de la actividad superficial y buena resistencia al agua dura (tolerancia a los iones de calcio).
Según las propiedades tensioactivas de los aminoácidos (por ejemplo, la tensión superficial, CMC, el comportamiento de fase y la temperatura de Krafft), se alcanzaron las siguientes conclusiones después de estudios extensos: la actividad superficial de AAS es superior a la de su contraparte tensioactiva convencional.
6.1 Concentración crítica de micelas (CMC)
La concentración crítica de las micelas es uno de los parámetros importantes de los tensioactivos y gobierna muchas propiedades activas de superficie, como la solubilización, la lisis celular y su interacción con las biopelículas, etc. En general, aumentando la longitud de la cadena de la cola de hidrocarburos (aumentando la hidrofobicidad) conduce a una disminución en el valor CMC de la solución de tensioactivo, aumentando así su actividad superficial. Los tensioactivos basados en aminoácidos generalmente tienen valores de CMC más bajos en comparación con los tensioactivos convencionales.
A través de diferentes combinaciones de grupos de cabeza y colas hidrófobas (amida monociónica, amida bi-cacante, éster a base de amida bi-cacio), Infante et al. Sintetizó tres AA basados en arginina y estudió sus CMC y γCMC (tensión superficial en CMC), lo que demuestra que los valores de CMC y γCMC disminuyeron al aumentar la longitud de la cola hidrofóbica. En otro estudio, Singare y Mhatre encontraron que el CMC de los tensioactivos N-α-acucinina disminuyó al aumentar el número de átomos de carbono de cola hidrofóbica (Tabla 1).
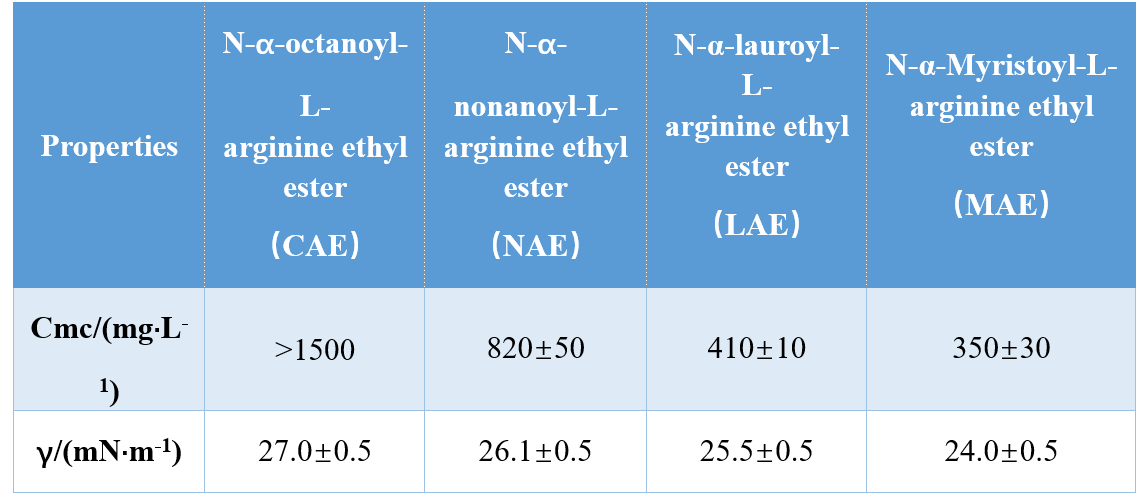
Yoshimura et al. Investigó el CMC de los tensioactivos de Géminis basados en aminoácidos derivados de cisteína y demostró que el CMC disminuyó cuando la longitud de la cadena de carbono en la cadena hidrofóbica aumentó de 10 a 12. El aumento de la longitud de la cadena de carbono a 14 resultó en un aumento en el CMC, lo que confirmó que los tensiones gemini de cadena larga tienen una tendencia menor a agregado.
Faustino et al. informó la formación de micelas mixtas en soluciones acuosas de tensioactivos aniónicos de Géminis basados en cistina. Los tensioactivos de Géminis también se compararon con los tensioactivos monoméricos convencionales correspondientes (C 8 Cys). Se informó que los valores de CMC de las mezclas de superficie de lípidos eran más bajos que los de los tensioactivos puros. Los tensioactivos de Géminis y la fosfolina 1,2-diheptanoil-Sn-gliceril-3-fosfocolina, un fosfolípido de micela soluble en agua, tenían CMC en el nivel milimolar.
Shrestha y Aramaki investigaron la formación de micelas viscoelásticas similares a gusanos en soluciones acuosas de tensioactivos aniónicos noónicos basados en aminoácidos mixtos en ausencia de sales de mezcla. En este estudio, se encontró que el glutamato de N-dodecil tenía una temperatura de Krafft más alta; Sin embargo, cuando se neutralizó con el aminoácido básico L-lisina, generó micelas y la solución comenzó a comportarse como un líquido newtoniano a 25 ° C.
6.2 Buena solubilidad de agua
La buena solubilidad de agua de AAS se debe a la presencia de enlaces CO-NH adicionales. Esto hace que AAS sea más biodegradable y ecológica que los tensioactivos convencionales correspondientes. La solubilidad de agua del ácido N-acil-L-glutámico es aún mejor debido a sus 2 grupos carboxilo. La solubilidad en el agua de CN (CA) 2 también es buena porque hay 2 grupos de arginina iónica en la molécula 1, lo que da como resultado una adsorción y difusión más efectiva en la interfaz celular e incluso una inhibición bacteriana efectiva a concentraciones más bajas.
6.3 Krafft Temperatura y Krafft Point
La temperatura de Krafft puede entenderse como el comportamiento de solubilidad específico de los tensioactivos cuya solubilidad aumenta bruscamente por encima de una temperatura particular. Los tensioactivos iónicos tienden a generar hidratos sólidos, lo que puede precipitar fuera del agua. A una temperatura particular (la llamada temperatura de Krafft), generalmente se observa un aumento dramático y discontinuo en la solubilidad de los tensioactivos. El punto Krafft de un tensioactivo iónico es su temperatura de Krafft en CMC.
Esta característica de solubilidad generalmente se ve para los tensioactivos iónicos y puede explicarse de la siguiente manera: la solubilidad del monómero libre de tensioactivos se limita por debajo de la temperatura de Krafft hasta que se alcanza el punto Krafft, donde aumenta su solubilidad gradualmente debido a la formación de micelas. Para garantizar la solubilidad completa, es necesario preparar formulaciones de tensioactivos a temperaturas por encima del punto de Krafft.
La temperatura de Krafft de AAS se ha estudiado y comparado con la de los tensioactivos sintéticos convencionales. Shrestha y Aramaki estudiaron la temperatura de Krafft de AAS a base de arginina y descubrieron que la concentración crítica de micelas exhibía un comportamiento de agregación en la formación de los tipos de medidas de medidas anteriores de 2-5 × 10-6 mol-1 seguidas por la formación normal (OHTA et al. AAS y discutió la relación entre su temperatura de Krafft y los residuos de aminoácidos.
En los experimentos, se descubrió que la temperatura de Krafft de N-hexadecanoil aas aumentó con la disminución del tamaño de los residuos de aminoácidos (la fenilalanina es una excepción), mientras que el calor de solubilidad (absorción de calor) aumentó con el tamaño decreciente de los residuos de aminoácidos (con la excepción de la glicina y la fenilanina). Se concluyó que en los sistemas de alanina y fenilalanina, la interacción DL es más fuerte que la interacción LL en la forma sólida de la sal de N-hexadecanoil aas.
Brito et al. determinó la temperatura de Krafft de tres series de tensioactivos nuevos a base de aminoácidos que utilizan microcalorimetría de escaneo diferencial y descubrieron que cambiar el ion trifluoroacetato a ion yoduro dio como resultado un aumento significativo en la temperatura de Krafft (aproximadamente 6 ° C), de 47 ° C a 53 ° C. La presencia de enlaces cis-dobles y la insaturación presente en los derivados de la cadena larga condujo a una disminución significativa en la temperatura de Krafft. Se informó que el glutamato de N-dodecilo tenía una temperatura de Krafft más alta. Sin embargo, la neutralización con el aminoácido básico L-lisina dio como resultado la formación de micelas en solución que se comportaron como fluidos newtonianos a 25 ° C.
6.4 Tensión superficial
La tensión superficial de los tensioactivos está relacionada con la longitud de la cadena de la parte hidrofóbica. Zhang et al. Determinado la tensión superficial del método de placa de sodio de cocoil por el método de placa de Wilhelmy (25 ± 0.2) ° C y determinó el valor de la tensión superficial en CMC como 33 mn -M -1, CMC como 0.21 mmol -L -1. Yoshimura et al. determinó la tensión superficial de la tensión superficial de la superficie a base de aminoácidos 2c n Cys de los agentes activos de la superficie basados en 2C N Cys. Se encontró que la tensión superficial en CMC disminuyó al aumentar la longitud de la cadena (hasta n = 8), mientras que la tendencia se invirtió para tensioactivos con n = 12 o longitudes de cadena más largas.
También se ha estudiado el efecto de CAC1 2 en la tensión superficial de los tensioactivos basados en aminoácidos dicarboxilados. En estos estudios, se añadió CAC1 2 a soluciones acuosas de tres tensioactivos de tipo aminoácidos dicarboxilados (C12 Malna 2, C12 Aspna 2 y C12 Gluna 2). Los valores de la meseta después de CMC se compararon y se encontró que la tensión superficial disminuyó a concentraciones de Cac1 2 muy bajas. Esto se debe al efecto de los iones de calcio en la disposición del tensioactivo en la interfaz de agua de gas. Las tensiones superficiales de las sales de N-dodecilaminomalonato y N-dodecilpartato, por otro lado, también fueron casi constantes hasta 10 mmol-L -1 CAC1 2. Por encima de 10 mmol -L -1, la tensión superficial aumenta bruscamente, debido a la formación de una precipitación de la sal de calcio del tensioactivo. Para la sal del disódico del glutamato N-dodecilo, la adición moderada de Cac1 2 dio como resultado una disminución significativa en la tensión superficial, mientras que el aumento continuo en la concentración de Cac1 2 ya no causó cambios significativos.
Para determinar la cinética de adsorción de los AA de tipo Gemini en la interfaz de agua de gas, la tensión superficial dinámica se determinó utilizando el método máximo de presión de burbuja. Los resultados mostraron que durante el tiempo de prueba más largo, la tensión superficial dinámica 2C 12 Cys no cambió. La disminución de la tensión superficial dinámica depende solo de la concentración, la longitud de las colas hidrofóbicas y el número de colas hidrofóbicas. El aumento de la concentración de tensioactivo, la disminución de la longitud de la cadena, así como el número de cadenas, dio como resultado una descomposición más rápida. Se encontró que los resultados obtenidos para concentraciones más altas de C N (n = 8 a 12) estaban muy cerca del γ CMC medido por el método Wilhelmy.
En otro estudio, las tensiones de superficie dinámica de la cistina de sodio cistina (SDLC) y la cistina didecamino de sodio se determinaron mediante el método de la placa de Wilhelmy, y además, las tensiones de la superficie de equilibrio de sus soluciones acuosas se determinaron por el método de volumen de caída. La reacción de los bonos disulfuro fue investigada por otros métodos también. La adición de mercaptoetanol a 0.1 mmol -L -1SDLC solución condujo a un rápido aumento en la tensión superficial de 34 mn -m -1 a 53 mn -m -1. Dado que NACLO puede oxidar los enlaces disulfuro de SDLC a grupos de ácido sulfónico, no se observaron agregados cuando se añadió NACLO (5 mmol -L -1) a la solución SDLC de 0,1 mmol -L -1. La microscopía electrónica de transmisión y los resultados de dispersión de luz dinámica mostraron que no se formaron agregados en la solución. Se encontró que la tensión superficial de SDLC aumenta de 34 mn -m -1 a 60 mn -m -1 durante un período de 20 min.
6.5 Interacciones de superficie binaria
En las ciencias de la vida, varios grupos han estudiado las propiedades vibratorias de las mezclas de AAS catiónicas (tensioactivos a base de diacilglicerol arginina) y fosfolípidos en la interfaz de agua de gas, lo que finalmente concluye que esta propiedad no ideal provoca la prevalencia de las interacciones electrostáticas.
6.6 Propiedades de agregación
La dispersión de la luz dinámica se usa comúnmente para determinar las propiedades de agregación de los monómeros a base de aminoácidos y los tensioactivos de Géminis a concentraciones superiores a CMC, produciendo un aparente diámetro hidrodinámico DH (= 2R H). Los agregados formados por C n Cys y 2Cn Cys son relativamente grandes y tienen una distribución a gran escala en comparación con otros tensioactivos. Todos los tensioactivos, excepto 2C 12 Cys, generalmente forman agregados de aproximadamente 10 nm. Los tamaños de micelas de los tensioactivos de Géminis son significativamente más grandes que los de sus homólogos monoméricos. Un aumento en la longitud de la cadena de hidrocarburos también conduce a un aumento en el tamaño de las micelas. Ohta et al. describió las propiedades de agregación de tres estereoisómeros diferentes de N-dodecil-fenil-alanil-fenilalalal-alanina tetrametilamonio en solución acuosa y mostraron que los diastereoisómeros tienen la misma concentración de agregación crítica en la solución acuosa. Iwahashi et al. investigated by circular dichroism, NMR and vapor pressure osmometry the The formation of chiral aggregates of N-dodecanoyl-L-glutamic acid, N-dodecanoyl-L-valine and their methyl esters in different solvents (such as tetrahydrofuran, acetonitrile, 1,4-dioxane and 1,2-dichloroethane) with rotational properties was investigated by Dicroísmo circular, RMN y osmometría de presión de vapor.
6.7 Adsorción interfacial
La adsorción interfacial de tensioactivos a base de aminoácidos y su comparación con su contraparte convencional también es una de las direcciones de investigación. Por ejemplo, se investigaron las propiedades de adsorción interfacial de los ésteres de dodecilo de los aminoácidos aromáticos obtenidos de LET y LEP. Los resultados mostraron que LET y LEP exhibieron áreas interfaciales más bajas en la interfaz de gas líquido y en la interfaz de agua/hexano, respectivamente.
Bordes et al. Investigó el comportamiento de la solución y la adsorción en la interfaz de agua de gas de tres tensioactivos de aminoácidos dicarboxilados, las sales de disodio del glutamato de dodecilo, el dodecil aspartato y el aminomalonato (con 3, 2 y 1 átomos de carbono entre los dos grupos carboxilo, respectivamente). Según este informe, el CMC de los tensioactivos dicarboxilados fue 4-5 veces mayor que el de la sal monocarboxilada de dodecilglicina. Esto se atribuye a la formación de enlaces de hidrógeno entre los tensioactivos dicarboxilados y las moléculas vecinas a través de los grupos de amida en el mismo.
6.8 Comportamiento de fase
Se observan fases cúbicas discontinuas isotrópicas para tensioactivos a concentraciones muy altas. Las moléculas tensioactivas con grupos de cabeza muy grandes tienden a formar agregados de curvatura positiva más pequeña. Marques et al. Estudió el comportamiento de fase de los sistemas 12ys12/12ser y 8lys8/16Ser (ver Figura 10), y los resultados mostraron que el sistema 12 -3ys12/12Ser tiene una zona de separación de fases entre las regiones de soluciones micelares y vesiculares, mientras que la región de la fase de la fase de la Micellar 8 de los 8 años 8/16 muestra la región de la fase de la vesícula. región). Cabe señalar que para la región de la vesícula del sistema 12ys12/12ser, las vesículas siempre coexisten con micelas, mientras que la región de la vesícula del sistema 8lys8/16ser solo tiene vesículas.
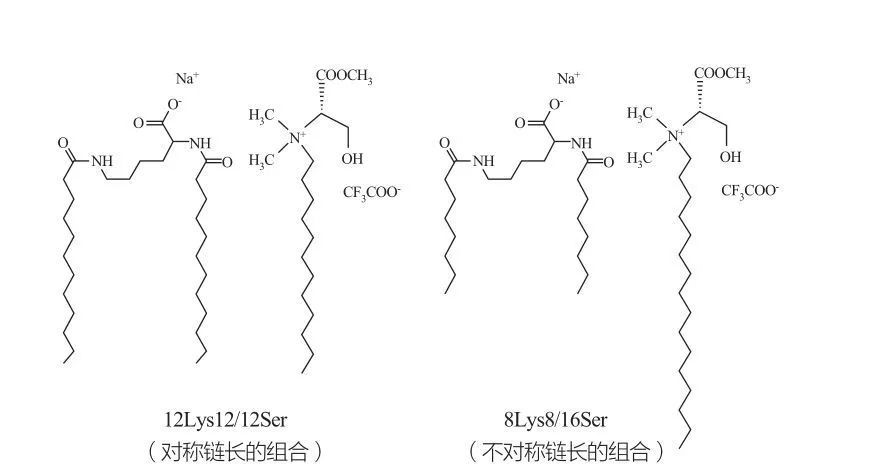
Mezclas catanionicas de los tensioactivos a base de lisina y serina: par symetric 12lys12/12ser (izquierda) y par 8 lys8/16ser asimétrico (derecha)
6.9 Capacidad de emulsionante
Kouchi et al. examinó la capacidad de emulsionamiento, la tensión interfacial, la dispersión y la viscosidad de N- [3-dodecil-2-hidroxipropil] -L-arginina, L-glutamato y otros AA. En comparación con los tensioactivos sintéticos (sus homólogos no iónicos y anfotéricos convencionales), los resultados mostraron que los AA tienen una capacidad emulsionante más fuerte que los tensioactivos convencionales.
Baczko et al. Nuevos tensioactivos de aminoácidos aniónicos sintetizados e investigaron su idoneidad como solventes de espectroscopía de RMN orientado a quiral. Se sintetizaron una serie de derivados de L-PHE o L-ALA a base de sulfonato con diferentes colas hidrofóbicas (pentil ~ tetradecilo) reaccionando aminoácidos con anhídrido O-sulfobenzoico. Wu et al. sales de sodio sintetizadas de acil aas y grasas yinvestigó su capacidad de emulsificación en las emulsiones de aceite en agua, y los resultados mostraron que estos tensioactivos tuvieron un mejor rendimiento con el acetato de etilo como fase de aceite que con el n-hexano como fase de aceite.
6.10 Avances en síntesis y producción
La resistencia al agua dura puede entenderse como la capacidad de los tensioactivos para resistir la presencia de iones como el calcio y el magnesio en agua dura, es decir, la capacidad de evitar la precipitación en los jabones de calcio. Los tensioactivos con alta resistencia al agua dura son muy útiles para formulaciones de detergentes y productos de cuidado personal. La resistencia al agua dura se puede evaluar calculando el cambio en la solubilidad y la actividad superficial del tensioactivo en presencia de iones de calcio.
Otra forma de evaluar la resistencia al agua dura es calcular el porcentaje o gramos de tensioactivo requerido para el jabón de calcio formado a partir de 100 g de oleado de sodio para dispersarse en el agua. En áreas con agua dura alta, las altas concentraciones de iones de calcio y magnesio y el contenido mineral pueden dificultar algunas aplicaciones prácticas. A menudo, el ion de sodio se usa como contrarresta de un tensioactivo aniónico sintético. Dado que el ion de calcio divalente está vinculado a ambas moléculas tensioactivas, hace que el tensioactivo precipite más fácilmente de la solución, lo que hace que la detergencia sea menos probable.
El estudio de la resistencia al agua dura de AAS mostró que la resistencia al ácido y el agua dura estaban fuertemente influenciadas por un grupo carboxilo adicional, y la resistencia ácida y del agua dura aumentó aún más con el aumento de la longitud del grupo espaciador entre los dos grupos carboxilo. El orden de resistencia ácida y del agua dura fue C 12 glicinato <C 12 Aspartato <C 12 Glutamato. Comparando el enlace de amida dicarboxilado y el tensioactivo amino dicarboxilado, respectivamente, se encontró que el rango de pH de este último era más amplio y su actividad superficial aumentó con la adición de una cantidad apropiada de ácido. Los aminoácidos n-al alquilados diicarboxilados mostraron un efecto quelante en presencia de iones de calcio, y C 12 se formó un gel blanco formado por aspartato. C 12 El glutamato mostró una alta actividad superficial a alta concentración de Ca 2+ y se espera que se use en la desalinización del agua de mar.
6.11 Dispersibilidad
La dispersión se refiere a la capacidad de un tensioactivo para evitar la coalescencia y la sedimentación del tensioactivo en solución.La dispersión es una propiedad importante de los tensioactivos que los hace adecuados para su uso en detergentes, cosméticos y productos farmacéuticos.Un agente disperso debe contener un éster, éter, amida o unión amino entre el grupo hidrofóbico y el grupo hidrofílico terminal (o entre los grupos hidrofóbicos de cadena recta).
En general, los tensioactivos aniónicos como el alkanolamido sulfatos y los tensioactivos anfotéricos como la amidosulfobetaína son particularmente efectivos como agentes dispersantes para los jabones de calcio.
Muchos esfuerzos de investigación han determinado la dispersión de AAS, donde se encontró que N-Lauroil lisina era poco compatible con el agua y difícil de usar para las formulaciones cosméticas.En esta serie, los aminoácidos básicos sustituidos con N-acil tienen una dispersión excelente y se utilizan en la industria cosmética para mejorar las formulaciones.
07 toxicidad
Los tensioactivos convencionales, especialmente los tensioactivos catiónicos, son altamente tóxicos para los organismos acuáticos. Su toxicidad aguda se debe al fenómeno de la interacción de iones de adsorción de los tensioactivos en la interfaz de agua celular. La disminución del CMC de los tensioactivos generalmente conduce a una adsorción interfacial más fuerte de tensioactivos, lo que generalmente resulta en su toxicidad aguda elevada. Un aumento en la longitud de la cadena hidrofóbica de los tensioactivos también conduce a un aumento en la toxicidad aguda de tensioactivo.La mayoría de los AA son bajos o no tóxicos para los humanos y el medio ambiente (especialmente para los organismos marinos) y son adecuados para su uso como ingredientes alimentarios, farmacéuticos y cosméticos.Muchos investigadores han demostrado que los tensioactivos de aminoácidos son suaves y no irritantes para la piel. Se sabe que los tensioactivos a base de arginina son menos tóxicos que sus homólogos convencionales.
Brito et al. estudió las propiedades fisicoquímicas y toxicológicas de los anfifílicos a base de aminoácidos y sus [derivados de tirosina (Tyr), hidroxiprolina (HYP), serina (SER) y lisina (Lys)] Formación espontánea de vesículas cátionarias y dieron datos sobre su toxicidad aguda a Daphnia Magna (IC 50). Sintetizaron vesículas catiónicas de bromuro de dodeciltrimetilamonio (DTAB)/derivados de Lys y/o mezclas derivadas de SER/LYS y probaron su ecotoxicidad y potencial hemolítico, mostrando que todas las mezclas que contienen vesículas eran menos tóxicas que el DTAB tóxico convencional.
Rosa et al. investigó la unión (asociación) de ADN a vesículas catiónicas basadas en aminoácidos estables. A diferencia de los tensioactivos catiónicos convencionales, que a menudo parecen ser tóxicos, la interacción de los tensioactivos de aminoácidos catiónicos parece no ser tóxico. El AAS catiónico se basa en arginina, que forma espontáneamente vesículas estables en combinación con ciertos tensioactivos aniónicos. También se informa que los inhibidores de corrosión a base de aminoácidos no son tóxicos. Estos tensioactivos se sintetizan fácilmente con alta pureza (hasta 99%), bajo costo, fácilmente biodegradable y completamente soluble en medios acuosos. Varios estudios han demostrado que los tensioactivos de aminoácidos que contienen azufre son superiores en la inhibición de la corrosión.
En un estudio reciente, Perinelli et al. informó un perfil toxicológico satisfactorio de los ramnolípidos en comparación con los tensioactivos convencionales. Se sabe que los ramnolípidos actúan como potenciadores de permeabilidad. También informaron el efecto de los ramnolípidos sobre la permeabilidad epitelial de los medicamentos macromoleculares.
08 actividad antimicrobiana
La actividad antimicrobiana de los tensioactivos puede evaluarse mediante la concentración inhibitoria mínima. La actividad antimicrobiana de los tensioactivos a base de arginina se ha estudiado en detalle. Se encontró que las bacterias gramnegativas son más resistentes a los tensioactivos a base de arginina que las bacterias Gram-positivas. La actividad antimicrobiana de los tensioactivos generalmente aumenta por la presencia de enlaces hidroxilo, ciclopropano o insaturados dentro de las cadenas de acilo. Castillo et al. demostró que la longitud de las cadenas de acilo y la carga positiva determinan el valor de HLB (equilibrio hidrofílico-lipófilo) de la molécula, y estos tienen un efecto en su capacidad para interrumpir las membranas. El éster metílico de Nα-acucinina es otra clase importante de tensioactivos catiónicos con actividad antimicrobiana de amplio espectro y es fácilmente biodegradable y tiene baja o toxicidad. Estudios sobre la interacción de los tensioactivos basados en el éster de metilo de Nα-acucinina con 1,2-dipalmitoil-Sn-propiltrioxil-3-fosforilcolina y 1,2-ditetradecanoil-propiltrioxiloxil-3-fosforilcolina, las membranas modelo y con los organismos vivientes en la presencia o ausencia de los barrieras externos han demostrado que esto tiene la base de los surfactores de los barrijos externos ha demostrado que esto ha demostrado esto. Antimicrobiano Los resultados mostraron que los tensioactivos tienen buena actividad antibacteriana.
09 propiedades reológicas
Las propiedades reológicas de los tensioactivos juegan un papel muy importante en la determinación y la predicción de sus aplicaciones en diferentes industrias, incluidos alimentos, productos farmacéuticos, extracción de aceite, cuidado personal y productos para el cuidado del hogar. Se han realizado muchos estudios para discutir la relación entre la viscoelasticidad de los tensioactivos de aminoácidos y CMC.
10 aplicaciones en la industria cosmética
Los AA se utilizan en la formulación de muchos productos de cuidado personal.Se encuentra que el glicinato de potasio N-cocoil es suave con la piel y se usa en la limpieza facial para eliminar el lodo y el maquillaje. El ácido N-acil-L-glutámico tiene dos grupos carboxilo, lo que lo hace más soluble en agua. Entre estos AA, los AA basados en los ácidos grasos C 12 se usan ampliamente en la limpieza facial para eliminar el lodo y el maquillaje. Los AA con una cadena C 18 se utilizan como emulsionantes en productos para el cuidado de la piel, y se sabe que las sales de alanina de N-laurilo crean espumas cremosas que no son irritantes para la piel y, por lo tanto, pueden usarse en la formulación de productos para el cuidado del bebé. Los AA a base de N-laurilo utilizado en la pasta de dientes tienen una buena detergencia similar al jabón y una fuerte eficacia en la enzima inhibición de la enzima.
En las últimas décadas, la elección de tensioactivos para cosméticos, productos de cuidado personal y productos farmacéuticos se ha centrado en la baja toxicidad, la suavidad, la gentileza al tacto y la seguridad. Los consumidores de estos productos son muy conscientes de la posible irritación, toxicidad y factores ambientales.
Hoy, los AA se utilizan para formular muchos champús, tintes para el cabello y jabones de baño debido a sus muchas ventajas sobre sus contrapartes tradicionales en cosméticos y productos de cuidado personal.Los tensioactivos basados en proteínas tienen propiedades deseables necesarias para productos de cuidado personal. Algunos AA tienen capacidades de formación de películas, mientras que otras tienen buenas capacidades de espuma.
Los aminoácidos son importantes factores hidratantes naturales en el estrato córneo. Cuando las células epidérmicas mueren, se convierten en parte del estrato córneo y las proteínas intracelulares se degradan gradualmente a los aminoácidos. Estos aminoácidos se transportan más al estrato córneo, donde absorben sustancias de grasa o de grasa en el estrato córneo epidérmico, mejorando así la elasticidad de la superficie de la piel. Aproximadamente el 50% del factor hidratante natural en la piel está compuesto de aminoácidos y pirrolidona.
El colágeno, un ingrediente cosmético común, también contiene aminoácidos que mantienen la piel suave.Los problemas de la piel, como la aspereza y la opacidad, se deben en gran parte a la falta de aminoácidos. Un estudio mostró que mezclar un aminoácido con un ungüento alivio de las quemaduras de la piel, y las áreas afectadas volvieron a su estado normal sin convertirse en cicatrices queloides.
También se ha encontrado que los aminoácidos son muy útiles para el cuidado de las cutículas dañadas.El cabello seco y sin forma puede indicar una disminución en la concentración de aminoácidos en un estrato córneo severamente dañado. Los aminoácidos tienen la capacidad de penetrar la cutícula en el tallo del cabello y absorber la humedad de la piel.Esta capacidad de los tensioactivos a base de aminoácidos los hace muy útiles en champús, tintes para el cabello, suavizantes del cabello, acondicionadores del cabello y la presencia de aminoácidos fortalece el cabello.
11 Aplicaciones en cosméticos cotidianos
Actualmente, existe una creciente demanda de formulaciones de detergentes basadas en aminoácidos en todo el mundo.Se sabe que los AA tienen una mejor capacidad de limpieza, capacidad de espuma y propiedades de ablandamiento de telas, lo que los hace adecuados para detergentes para el hogar, champús, lavados corporales y otras aplicaciones.Se informa que un AAS anfotérico derivado del ácido aspártico es un detergente altamente efectivo con las propiedades quelantes. Se descubrió que el uso de ingredientes detergentes que consisten en ácidos N-alquil-β-aminoetoxi reducen la irritación de la piel. Se ha informado que una formulación de detergente líquido que consiste en N-cocoil-β-aminopropionato es un detergente efectivo para las manchas de aceite en las superficies metálicas. También se ha demostrado que un tensioactivo de ácido aminocarboxílico, C 14 Chohch 2 NHCH 2 Coona, tiene una mejor detergencia y se usa para limpiar textiles, alfombras, cabello, vidrio, etc. La 2-hidroxi-3-aminopropionic ácido-N, el ácido N-acetoacético El derivado de derivados es conocido para tener una buena capacidad de complejación y la estabilidad a la estabilidad a los agentes de la blanqueamiento.
Keigo y Tatsuya han informado de la preparación de formulaciones de detergente basadas en N- (acil-alanilo-alanilo)-alanina-alanina en su patente para una mejor capacidad de lavado y estabilidad, ruptura de espuma fácil y buen ablandamiento de telas. KAO desarrolló una formulación de detergente basada en N-acil-1 -N-hidroxi-β-alanina e informó irritación de la piel baja, alta resistencia al agua y alta potencia de eliminación de manchas.
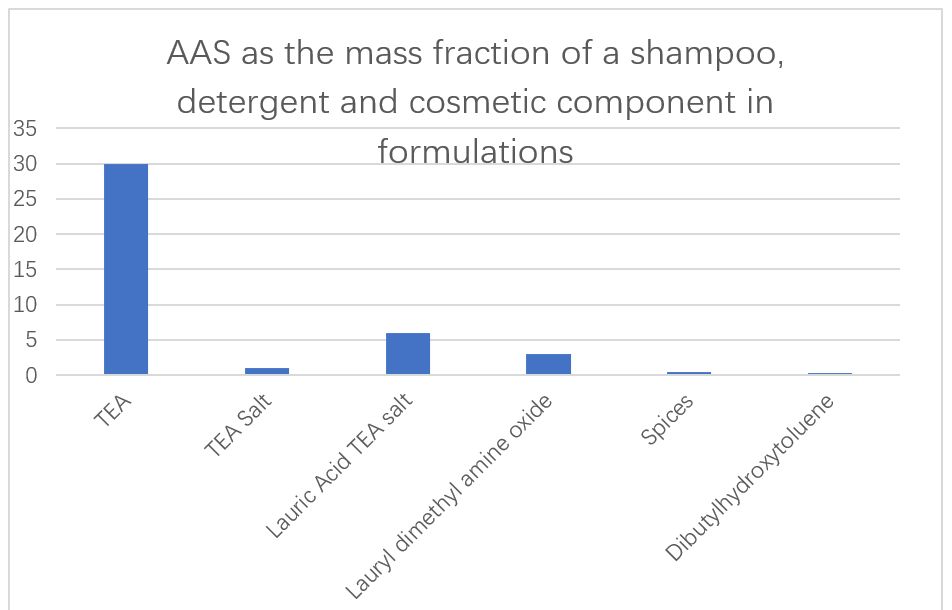
La compañía japonesa Ajinomoto utiliza AA de baja tóxica y fácilmente degradable basada en el ácido L-glutámico, L-arginina y L-lisina como ingredientes principales en champús, detergentes y cosméticos (Figura 13). También se ha informado la capacidad de los aditivos enzimáticos en las formulaciones de detergentes para eliminar el ensuciamiento de proteínas. Se ha informado que el N-acil aas derivado del ácido glutámico, la alanina, la metilglicina, la serina y el ácido asparto para su uso como excelentes detergentes líquidos en soluciones acuosas. Estos tensioactivos no aumentan la viscosidad en absoluto, incluso a temperaturas muy bajas, y pueden transferirse fácilmente desde el recipiente de almacenamiento del dispositivo de espuma para obtener espumas homogéneas.
Tiempo de publicación: Jun-09-2022

